| 您所在的位置: 网络辟谣举报平台 > 百科常识 |
传言:
新冠病毒检测试剂盒出家用自测版。
辟谣:
胶体金法的抗体检测试剂操作简便,类似于早早孕检测试剂,可能因此被误认为是所谓的“家用自测版”,但实际上,国家批准的用途明确规定只能是医疗机构使用,不适合一般人群使用,原因在于采集血样需要一定条件、试验需要相应温度湿度、结果判定需要相应的专业知识(尤其是处于临界状态)。此外,任何检测试剂都是对疾病的辅助诊断。
目前,新冠病毒检测试剂盒分为病原体抗原、抗体和核酸检测试剂,属于第三类医疗器械,必须经国家药品监督管理局批准取得医疗器械注册证,这些经批准注册的新冠病毒检测试剂盒,均需要具备条件的实验室及专业的医疗机构才能完成检测,核酸检测试剂盒需要相应的专有检测设备,化学发光法的抗体检测试剂同样需要专有设备。因此,这类试剂盒切不可用来自行使用,更不能经由网络销售给消费者个人。
病原学试剂检测包括病毒核酸检测和病毒特异性抗原检测,试剂盒一般有免疫诊断与核酸检测两大类。
免疫诊断是应用抗原-抗体特异性结合原理,使用特定标记物进行分析检测的技术。免疫学检测一般有ELISA(酶联免疫吸附试验)、化学发光(CLIA)以及胶体金快速检测等,ELISA和化学发光检测时间也相对较长,检测灵敏度较高,一般需要30-120分钟;胶体金快速检测一般5-15分钟,检测灵敏度相对较低,不需专门的实验室和设备,适宜基层操作。
核酸检测是通过检测病原体特异性核酸序列来完成的,主要应用聚合酶链式反应,即通常所说的PCR检测,其优势在于极高灵敏度,同时特异性强、扩增环节自动化程度高,窗口期较短,一般3-5天(理论上核酸只要感染粘膜,就可以检测到),相对封闭的操作环境可以降低样本对环境的污染。核酸诊断包括:荧光定量PCR、数字PCR、高通量测序(NGS)和恒温扩增技术。
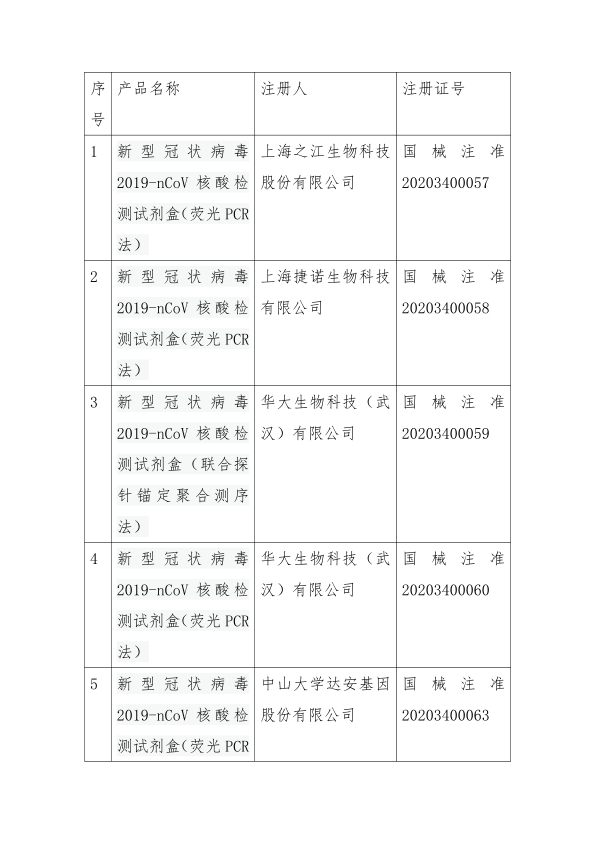
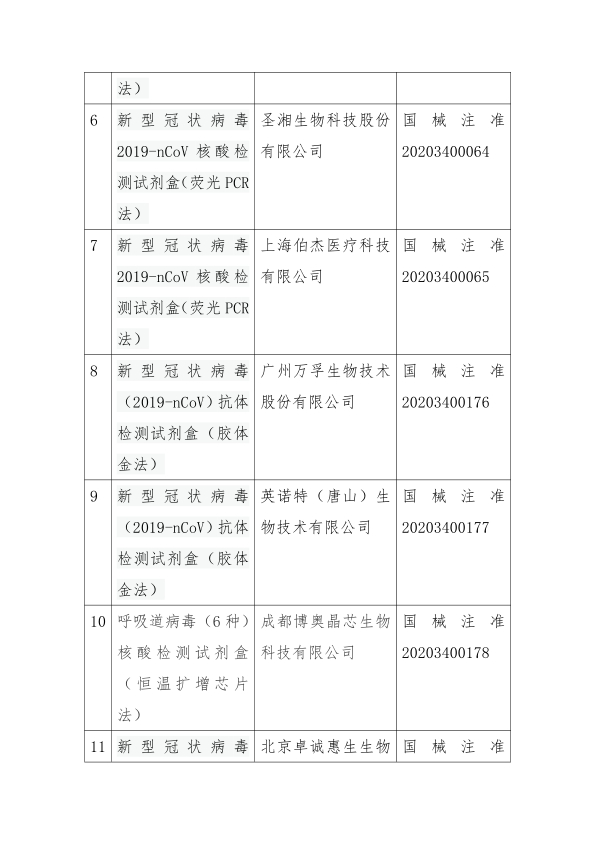
附件:国家已经批准的新冠检测试剂清单(截至3月6日)
国家目前已批准的新冠病毒检测试剂有11个产品,其中荧光PCR法8个,恒温扩增法1个,测序法1个,胶体金法2个,化学发光法3个。

辟谣专家:曾明 国家药典委员会疫苗专业委员会委员 研究员
复核专家:岳秉飞 中国食品药品检定研究院 研究员
| 欢迎扫码关注 |

| 闽辨真伪 |
| 联动辟谣 |